บทที่ 18 ความร้อน
ความร้อน
ความร้อนเป็นพลังงานรูปหนึ่งที่เปลี่ยนมาจากพลังงานรูปอื่น เช่น พลังงานไฟฟ้า พลังงานกล (พลังงานศักย์และพลังงานจลน์) พลังงานเคมี พลังงานนิวเคลียร์ หรืองาน เป็นต้น
พลังงานความร้อนมีหน่วยเป็นจูล (Joule, J ) ในระบบเอสไอ (SI) แต่บางครั้งอาจบอกเป็นหน่วยอื่นได้ เช่น แคลอรี (cal) และบีทียู (BTU)
พลังงานความร้อน 1 แคลอรี คือพลังงานความร้อนที่ทำให้น้ำมวล 1 กรัม มีอุณหภูเพิ่มขึ้น 1
องศาเซลเซียส (°C ) ในช่วง 14.5 °C ถึง 15.5 °C
พลังงานความร้อน 1 บีทียู คือ พลังงานความร้อนที่ทำให้น้ำที่มีมวล 1 ปอนด์ มีอุณหภูมิเพิ่มขึ้น 1
องศาฟาเรนไฮต์ (°F) ในช่วง 58.1 °F ถึง 59.1 °F
จากการทดลองพบว่า
1 cal = 4.186 J
1 BTU = 252 cal = 1055 J
อุณหภูมิ
นักวิทยาศาสตร์ได้กำหนดว่าอุณหภูมิ คือ ปริมาณที่แปรผันโดยตรงกับพลังงานจลน์เฉลี่ยของแก๊ส การที่เราจะบอกว่าวัตถุใดร้อนมากหรือน้อย เราสามารถบอกได้ด้วยอุณหภูมิของวัตถุนั้น คือ วัตถุที่มีระดับความร้อนมากจะมีอุณหภูมิสูง วัตถุที่มีระดับความร้อนน้อยจะมีอุณหภูมิต่ำ ดังนั้นถ้าเราเอาวัตถุที่มีอุณหภูมิสูงมาสัมผัสวัตถุที่มีอุณหภูมิต่ำ พลังงานความร้อนจะถูกถ่ายโอนจากวัตถุที่มีอุณหภูมิสูงไปยังวัตถุที่มีอุณหภูมิต่ำ จนวัตถุทั้งสองมีอุณหภูมิเท่ากัน
อุปกรณ์ที่ใช้วัดอุณหภูมิเรียกว่า เทอร์โมมิเตอร์ เทอร์โมมิเตอร์มีหลายชนิด เช่น
1. สเกลองศาเซลเซียส (Celsuis, °C) หรือบางที่เรียกว่าองศาเซนติเกรด (ที่ความดัน 1 บรรยากาศ จุดเยือกแข็งของน้ำเป็น 0 เซลเซียสและจุดเดือดเป็น 100 เซลเซียส ระหว่างจุดเยือกแข็งและจุดเดือดแบ่งเป็น 100 ส่วนเท่าๆ กัน )
2. สเกลองศาเคลวิน (Kelvin, °K) เป็นหน่วยของอุณหภูมิสัมบูรณ์ (ที่ความดัน 1 บรรยากาศ จุดเยือกแข็งของน้ำเป็น 273.16 เคลวินและจุดเดือดเป็น 373.16 เคลวิน ระหว่างจุดเยือกแข็งและจุดเดือดแบ่งเป็น 100 ส่วนเท่าๆ กัน ) ##หน่วยเคลวินเป็นหน่วยมาตรฐานในระบบเอสไอ
ปริมาณความร้อนของวัตถุ (HEAT, Q)
เป็นพลังงานความร้อนที่วัตถุรับเข้ามาหรือคายออกไป จากการศึกษาผลของความร้อนต่อสสารหรือวัตถุในชั้นนี้จะศึกษาเพียงสองด้าน คือ
1. ความร้อนจำเพาะ ( Specific heat ) หมายถึง พลังงานความร้อนที่ทำให้วัตถุมีอุณหภูมิสูงขึ้นหรือต่ำลงโดยสถานะยังคงรูปเดิม
2. ความร้อนแฝง (Latent Heat) หมายถึง พลังงานความร้อนที่ทำให้วัตถุเปลี่ยนสถานะโดยอุณหภูมิคงที่
ความจุความร้อน ( Heat capacity, C ) คือความร้อนที่ทำให้สารทั้งหมดที่กำลังพิจารณามีอุณหภูมิเปลี่ยนไปหนึ่งหน่วย โดยสถานะไม่เปลี่ยน
ถ้าให้ปริมาณความร้อน ΔQ แก่วัตถุ ทำให้อุณหภูมิของวัตถุเปลี่ยนไป ΔT ดังนั้นถ้าอุณหภูมิของวัตถุเปลี่ยนไป 1 หน่วย จะใช้ความร้อน C คือ
ความจุความร้อนจำเพาะ (Specific Heat capacity , c ) คือความร้อนที่ทำให้สาร(วัตถุ) มวลหนึ่งหน่วยมีอุณหภูมิเปลี่ยนไปหนึ่งองศาเคลวิน คือ
นั่นคือ เมื่อสารมวล m มีอุณหภูมิเพิ่มจาก T1 เป็น T2 และความจุความร้อนจำเพาะมีค่าคงตัว ความร้อนที่สารได้รับ
คือ 
การเปลี่ยนสถานะของสาร
สารและสิ่งของที่อยู่รอบตัวเราจะพบว่ามีอยู่ 3 สถานะ คือ ของแข็ง (น้ำแข็ง) ของเหลว (น้ำ) และ
แก๊ส (ไอน้ำ) ได้
I. ของแข็ง แรงดึงดูดระหว่างโมเลกุลมีค่ามาก ทำให้โมเลกุลอยู่ใกล้กัน จึงทำให้รูปทรงของของแข็งไม่เปลี่ยนแปลงมากเมื่อมีแรงขนาดไม่มากนักมากระทำ ตามคำจำกัดความนี้ เหล็ก คอนกรีต ก้อนหิน เป็นของแข็ง
II. ของเหลว แรงดึงดูดระหว่างโมเลกุลมีค่าน้อย โมเลกุลจึงเคลื่อนที่ไปมาได้บ้าง จึงทำให้รูปทรงของของเหลวเปลี่ยนแปลงไปตามภาชนะที่ที่บรรจุ น้ำ น้ำมัน ปรอท เป็นของเหลว
III. แก๊ส แรงดึงดูดระหว่างโมเลกุลมีค่าน้อยมาก จนโมเลกุลของแก๊สอยู่ห่างกันมากและเคลื่อนที่ได้สะเปะสะปะ ฟุ้งกระจายเต็มภาชนะที่บรรจุ เช่นอากาศและแก๊สชนิดต่างๆ
สถานการณ์จำลอง แสดงให้เห็นการเปลี่ยนแปลงของสสาร( น้ำ ) เมื่อได้รับความร้อน
การขยายตัวของวัตถุเนื่องจากความร้อน
วัตถุโดยทั่วไปเมื่อได้รับความร้อนจะขยายตัว การขยายตัวของวัตถุจะขึ้นอยู่กับรูปร่างคือ
- วัตถุที่มีความยาวมีลักษณะเป็นเส้นหรือแท่งยาว จะมีการขยายตัวตามเส้น (การขยายตัวตามยาว)
- วัตถุที่เป็นแผ่นจะมีการขยายตัวตามพื้นที่
- วัตถุที่มีรูปร่างเป็นปริมาตรจะมีการขยายตัวตามปริมาตร
ในทางกลับกันถ้าวัตถุสูญเสียความร้อนก็จะหดตัว
สมบัติที่สำคัญๆ เกี่ยวกับการขยายของของแข็ง ได้แก่
1. ของแข็งต่างชนิดกัน ถ้าเดิมมีความยาวเท่ากัน เมื่อร้อนขึ้นเท่ากันจะมีส่วนขยายตัวเพิ่มขึ้นไม่เท่ากัน
2. ของแข็งชนิดเดียวกัน ถ้าเดิมมีความยาวเท่ากัน เมื่อร้อนขึ้นเท่ากันจะมีส่วนขยายตัวเพิ่มขึ้นเท่ากัน
3. การขยายตัวของวัตถุเป็นเรื่องที่สำคัญมากในทางวิศวกรรม เช่น การวางเหล็กรางรถไฟ การขึงสายไฟฟ้าแรงสูงเป็นต้น
ความร้อนจะถ่ายโอนหรือส่งผ่านจากวัตถุที่ระดับความร้อนสูง (อุณหภูมิสูง) ไปสู่วัตถุที่มีระดับความร้อนต่ำ (อุณหภูมิต่ำ) การถ่ายโอนความร้อนมี 3 แบบ คือ

รูป แสดงการถ่ายโอนความร้อนแบบต่าง ๆ
1. การนำ เป็นการถ่ายโอนพลังงานความร้อนผ่านตัวกลางซึ่งโดยมากจะเป็นพวกโลหะต่างๆ เช่น เราเอามือไปจับช้อนโลหะที่ปลายข้างหนึ่งแช่อยู่ในน้ำร้อน มือเราจะรู้สึกร้อน เพราะความร้อนถูกส่งผ่านจากน้ำร้อนมายังมือเราโดยมีช้อนโลหะเป็นตัวนำความร้อน
2. การพา เป็นการถ่ายโอนความร้อนโดยการเคลื่อนที่ของโมเลกุลของตัวกลางเป็นตัวพาความร้อนไปจากบริเวณที่ระดับความร้อนสูง (อุณหภูมิสูง) ไปสู่บริเวณที่มีระดับความร้อนต่ำ (อุณหภูมิต่ำ) เช่นเวลาต้มน้ำ ความร้อนจากเตาทำให้น้ำที่ก้นภาชนะร้อนจะขยายตัวทำให้มีความหนาแน่นน้อยกว่าน้ำด้านบนจึงลอยตัวสูงขึ้นส่วนน้ำด้านบนที่มีอุณหภูมิต่ำกว่าและความหนาแน่นมากก็จะจมลงมาแทนที่ การหมุนวนของน้ำทำให้เกิดการพาความร้อน
3. การแผ่รังสี เป็นการส่งพลังงานความร้อนที่อยู่ในรูปคลื่นแม่เหล็กไฟฟ้า (รังสีอินฟราเรด) ดังนั้นจึงไม่ต้องอาศัยตัวกลางในการเคลื่อนที่ เช่นการแผ่รังสีความร้อนจากดวงอาทิตย์มายังโลก โดยทั่วไปวัตถุที่แผ่รังสีได้ดีก็จะรับ(ดูดกลืน)รังสีได้ดีด้วย วัตถุชนิดนั้นเราเรียกว่าวัตถุดำ (Black Body) วัตถุดำไม่มีในธรรมชาติ มีแต่ในอุดมคติ ดังนั้นวัตถุที่มีลักษณะใกล้เคียงวัตถุดำคือ วัตถุที่มีสีดำ ในทางกลับกันวัตถุขาวจะไม่ดูดกลืนรังสีและ ไม่แผ่รังสีที่ตกกระทบ มีแต่ในอุดมคติเท่านั้น
สมดุลความร้อน
ปริมาณความร้อนที่วัตถุอุณหภูมิสูงคายออกมาหรือลดลง จะเท่ากับปริมาณความร้อนที่วัตถุอุณหภูมิต่ำได้รับเข้าไปหรือเพิ่มขึ้น ซึ่งอาจกล่าวสั้นๆ ว่า"ความร้อนลดเท่ากับความร้อนเพิ่ม"
อออออ หรือเขียนเป็นความสัมพันธ์ได้ว่า
ออออออออออออออออออออออvvvvvvvvอออออออออ ΔQลด = ΔQเพิ่ม

ขั้นตอนการแก้ปัญหาโจทย์เรื่องสมดุลความร้อน มีขั้นตอนดังนี้
1. แยกวัตถุออกเป็น 2 พวก คือ พวกอุณหภูมิสูงและพวกอุณหภูมิต่ำ แล้วเขียนแผนภาพ
2. หาปริมาณความร้อนที่วัตถุอุณหภูมิสูงลดลงหรือคายออกมาทั้งหมด หรืออาจเปลี่ยนสถานะ จาก ΔQ = mcΔT หรือ ΔQ = mL
3. หาปริมาณความร้อนที่วัตถุอุณหภูมิต่ำเพิ่มขึ้นหรือได้รับมาทั้งหมด หรืออาจเปลี่ยนสถานะ จาก ΔQ = mcΔT หรือ ΔQ = mL
4. ตั้งสมการ ΔQลด = ΔQเพิ่ม แล้วแทนค่า ΔQ ที่ได้จากข้อ 2 และข้อ 3 ลงในแต่ละข้างของสมการ
การประยุกต์ใช้
อออออ ความรู้เรื่องสมดุลความร้อนนั้นมีการนำมาประยุกต์ใช้งานอย่างแพร่หลาย ตัวอย่างหนึ่งที่เห็นได้ชัดเจน คือ ระบบระบายความร้อนไม่ว่าจะเป็นในรถยนต์ เครื่องปรับอากาศ หรือในระบบหนึ่งๆของโรงงานอุตสาหกรรม เรามักจะสังเกตได้ว่าโรงงานอุตสาหกรรมมักจะอยู่ใกล้แหล่งน้ำหรือมีบ่อพักน้ำขนาดใหญ่เพื่อกักเก็บน้ำไว้ใช้สำหรับระบบหล่อเย็นเครื่องจักรกลบางประเภท ท่านจะได้ศึกษาการคำนวณเกี่ยวกับระบบระบายความร้อนจากตัวอย่างต่อไปนี้
ตัวอย่าง โรงไฟฟ้าต้องการระบายความร้อนทิ้งในอัตรา 4000 kJ/s โดยใช้น้ำจากสระเป็นตัวรับความร้อนผ่านอุปกรณ์แลกเปลี่ยนความร้อน ซึ่งมีประสิทธิภาพในการแลกเปลี่ยนความร้อน 80% จงหาว่าน้ำในสระมีอุณหภูมิเริ่มต้น 20 °C และสระมีปริมาตร 1000 ลูกบาศก์เมตร ภายในเวลา 1 ชั่วโมง น้ำในสระจะมีอุณหภูมิเพิ่มขึ้นกีองศาเซลเซียส (ค่าความจุความร้อนจำเพาะของน้ำ 4 kj/kg.K และประสิทธิภาพในการแลกเปลี่ยนความร้อน คือ อัตราส่วนระหว่างปริมาณความร้อนที่ถ่ายเทจริงต่อปริมาณความร้อนสูงสุด)
วิธีทำ จากโจทย์วัตถุที่คายความร้อนออกมาคือโรงงานไฟฟ้า ส่วนวัตถุที่รับความร้อนเข้าไปคือน้ำในสระ โดยประสิทธิภาพในการแลกเปลี่ยนความร้อน 80% หมาบความว่า
ออออออออออออออออออออออออออออออออออ (80/100 )ΔQลด = ΔQเพิ่ม
หรือ ΔQน้ำ = (80/100)ΔQระบาย
mcΔT = 0.8 P.t
ρVΔT = 0.8 P.t (m=ρV และ P คือ พลังงานความร้อนที่ระบายออกต่อหน่วยเวลาหรืออัตราการระบายความร้อน)
1000 x 1000 x 4000 x ΔT = 0.8 x 4000 x 1000 x 3600
ΔT =2.9 °C
จากการทดลองและข้อสรุปของนักวิทยาศาสตร์หลายๆ คนที่ศึกษาเรื่องแก๊สเราจะเห็นว่า สมบัติของแก๊สมีความสัมพันธ์กันด้วยตัวแปรคล้ายๆ กัน คือ ทุกคนต่างก็ดูที่ปริมาตรของแก๊สที่เปลี่ยนไป ด้วยการกำหนดตัวแปรต้นแตกต่างกันออกไป
บอยล์ เมื่อเปลี่ยนความดันของแก๊ส ปริมาตรจะเป็นอย่างไร
ชาร์ล เมื่อเปลี่ยนอุณหภูมิของแก๊ส ปริมาตรจะเป็นอย่างไร
อาโวกาโดร เมื่อเปลี่ยนจำนวนโมลหรือจำนวนโมเลกุลของแก๊ส ปริมาตรจะเป็นอย่างไร
และทุกคนก็ได้ข้อสรุปดังที่ได้นำเสนอกฏของทุกคนมาแล้ว ถ้าเรารวบรวมกฎที่เกี่ยวกับแก๊สที่กล่าวมาแล้วทั้งหมด เราจะได้ความสัมพันธ์ดังนี้
จาก
กฏของบอยล์ 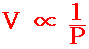
กฎของชาร์ล 
กฏของอาโวกาโดร 
เราสามารถรวมกฎทั้งสามนี้เข้าเป็นสมการรวมเพียงสมการเดียวได้ดังนี้
เมื่อ
| P = ความดัน |
| V = ปริมาตร |
| n = จำนวนโมล |
| T = อุณหภูมิ(เคลวิน,K) |
สมการนี้เรียกว่า สมการแก๊สในอุดมคติ
R = ค่าคงที่ของแก๊ส (gas constant)
จากตัวแปรทั้ง 4 ตัว คือ ความดัน(P), ปริมาตร(V), จำนวนโมล(n) และอุณหภูมิ(T) เราสามารถหาค่า R ได้จากการแทนค่าตัวแปรทั้งสี่ในสมการแก๊สอุดมคติ
แก๊สอุดมคติ 1 โมล ที่สภาวะมาตรฐาน ความดันเท่ากับ 1 บรรยากาศ อุณหภูมิ 273 K มีปริมาตร 22.4 ลิตร เราจะสามารถคำนวณหาค่าคงที่ของแก๊สได้ดังนี้
นอกจากนี้ค่าคงที่ R ยังมีได้อีกในหลายหน่วย ดังนี้
แก๊สใดๆ ก็ตามที่มีพฤติกรรมเป็นไปตามกฏนี้ จะเรียกแก๊สนั้นว่าแก๊สที่มีพฤติกรรมในอุดมคติ หรือแก๊สอุดมคติ หรือแก๊สสมบูรณ์แบบ (ideal gas)
ตัวอย่างการใช้กฎของแก๊สอุดมคติ ในการคำนวณ
ตัวอย่าง 1 น้ำจำนวน 1 กรัม ระเหยกลายเป็นไอในภาชนะขนาด 10 ลิตร ความดันของน้ำจะเป็นเท่าใดเมื่อการระเหยเป็นไอสมบูรณ์ที่อุณหภูมิ 200 องศาเซลเซียส
วิธีคำนวณ
จาก 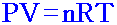
เราต้องการหาความดันของไอน้ำ
จำนวนโมล (n) ของน้ำ
และอุณหภูมิสัมบูรณ์ เท่ากับ
แทนค่า V = 10 L , T = 473 K และ n = 0.056 mol
ความดันจะเท่ากับ
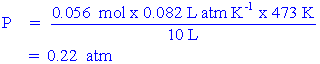
ตัวอย่าง 2 บอลลูนลูกหนึ่งบรรจุแก๊สฮีเลียม (He) หนัก 30 กิโลกรัม บอลลูนลูกนี้จะมีปริมาตรเท่าใด ถ้าความดันของแก๊สฮีเลียมเป็น 1.15 atm ณ อุณหภูมิ 20 องศาเซลเซียส
วิธีทำ
จาก 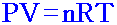
เราอยากทราบปริมาตรของบอลลูน
ก่อนอื่นต้องคำนวณหา จำนวนโมลของแก๊สฮีเลียม หนัก 30 กิโลกรัม ก่อน
เราทราบมาแล้วว่า ฮีเลียมจำนวน 1 โมล มีน้ำหนัก 4 กรัม หรือ 0.0040 kg
อุณหภูมิต้องเปลี่ยนเป็นหน่วยเคลวินก่อน
ดังนั้น ปริมาตรสามารถคำนวณได้ดังนี้
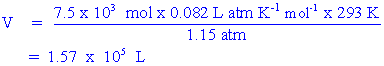
กฎของบอยล์ (Boyle's Law)
ทำให้โมเลกุลของแก๊สอยู่ใกล้กันมากขึ้น จึงเกิดการชนกันเองและชนผนังภาชนะมากขึ้น เป็นผลให้ความดันของแก๊สในกระบอกฉีดยาเพิ่มขึ้นเมื่อเทียบกับตอนเริ่มต้น ในทางตรงกันข้ามการเพิ่มปริมาตรของแก๊สในกระบอกฉีดยาทำให้โมเลกุลของแก๊สอยู่ห่างกัน การชนกันเองของโมเลกุลของแก๊สและการชนผนังภาชนะน้อยลง ความดันของแก๊สในกระบอกฉีดยาจึงลดลง
ถ้าปริมาตรของแก๊สเพิ่มขึ้นจะทำให้ความดันของแก๊สลดลง และเมื่อปริมาตรของแก๊สลดลง ความดันของแก๊สจะเพิ่มขึ้น

กฎของเกย์ ลูสแซก
ดังนั้น

กฎรวมแก๊ส ได้จากการนำเอากฎของบอยล์ กฎของชาร์ล มารวมกันจะได้ ความสัมพันธ์ของ P, V, T ดังนี้
กฎของบอยล์ V ∞ 1 เมื่ออุณหภูมิและมวลของแก๊สคงที่
P
กฎของชาร์ล V ∞ T เมื่อความดันและมวลของแก๊สคงที่
ดังนั้น V ∞ T
P
V = kT
P
PV = k
T
หรือ P1V1 = P2V2
T1 T2
ตัวอย่างที่ 1 แก๊สชนิดหนึ่งปริมาตร 3 dm3 บรรจุในภาชนะภายใต้ความดัน 740 mmHg
อุณหภูมิ 80 ํC ปริมาตรของแก๊สนี้ที่ STP จะเท่ากับกี่ลูกบาศก์เดซิเมตร
กฎของบอยล์ V ∞ 1 เมื่ออุณหภูมิและมวลของแก๊สคงที่
P
กฎของชาร์ล V ∞ T เมื่อความดันและมวลของแก๊สคงที่
ดังนั้น V ∞ T
P
V = kT
P
PV = k
T
หรือ P1V1 = P2V2
T1 T2
ตัวอย่างที่ 1 แก๊สชนิดหนึ่งปริมาตร 3 dm3 บรรจุในภาชนะภายใต้ความดัน 740 mmHg
อุณหภูมิ 80 ํC ปริมาตรของแก๊สนี้ที่ STP จะเท่ากับกี่ลูกบาศก์เดซิเมตร
วิธีทำ จากสูตร P1V1 = P2V2
T1 T2
740 mmHg X 3 dm3 = 760 mmHg X V2
273 + 80 K 273 K
740 mmHg X 3 dm3 = 760 mmHg X V2
353 K 273 K
V2 = 740mmHg X 3 dm3 X 273 K
353K X 760 mmHg
V2 = 2.26 dm3
T1 T2
740 mmHg X 3 dm3 = 760 mmHg X V2
273 + 80 K 273 K
740 mmHg X 3 dm3 = 760 mmHg X V2
353 K 273 K
V2 = 740
353
V2 = 2.26 dm3
ตัวอย่างที่ 2 แก๊สแอมโมเนียจำนวนหนึ่งวัดปริมาตรได้ 10 ลิตร ที่ 15 ํC และ 720 ทอรร์
จงหาปริมาตรของแก๊สนี้ถ้าเพิ่มอุณหภูมิเป็น 27 ํC และความดันเป็น 780 ทอรร์
วิธีทำ จากสูตร P1V1 = P2V2
T1 T2
720 torr X 10 L = 780 torr X V2
273 + 15 K 273 + 27 K
T1 T2
720 torr X 10 L = 780 torr X V2
273 + 15 K 273 + 27 K
720 torr X 10 L = 780 torr X V2
288 K 300 K
V2 = 720torr X 10 L X 300 K
288K X 780 torr
= 9.62 L
ปริมาตรของแก๊สนี้ = 9.62 ลิตร
288 K 300 K
V2 = 720
288
= 9.62 L
ปริมาตรของแก๊สนี้ = 9.62 ลิตร
ทฤษฎีจลน์ของแก๊ส
เป็นทฤษฎีที่ตั้งขึ้นเพื่อใช้อธิบายกฎ ปรากฏการณ์ หรือผลการทดลองที่เกี่ยวกับแก๊ส และพฤติกรรมของแก๊ส
1. แก๊สประกอบด้วยอนุภาคจำนวนมากที่มีขนาดเล็กมาก จนถือได้ว่าอนุภาคของแก๊สไม่มีปริมาตรเมื่อเทียบกับขนาดภาชนะที่บรรจุ
2. โมเลกุลของแก๊สอยู่ห่างกันมาก ทำให้แรงดึงดูดและแรงผลักระหว่างโมเลกุลน้อยมาก จนถือได้ว่าไม่มีแรงกระทำต่อกัน
3. โมเลกุลของแก๊สเคลื่อนที่อย่างรวดเร็วในแนวเส้นตรง เป็นอิสระ ด้วยอัตราเร็วคงที่ และไม่เป็นระเบียบ จนกระทั่งชนกับโมเลกุลอื่น ๆ หรือชนกับผนังภาชนะจึงจะเปลี่ยนทิศทางและอัตราเร็ว
4. โมเลกุลของแก๊สที่ชนกันเองหรือชนกับผนังภาชนะจะเกิดการถ่ายโอนพลังงานให้แก่กันได้ แต่พลังงานรวมของระบบคงที่
5. ณ อุณหภูมิเดียวกัน โมเลกุลของแก๊สแต่ละโมเลกุลเคลื่อนที่ด้วยอัตราเร็วไม่เท่ากัน แต่จะมีพลังงานจลน์เฉลี่ยเท่ากัน โดยที่พลังงานจลน์เฉลี่ยของแก๊สจะแปรผันตรงกับอุณหภูมิเคลวิน
+ แก๊สที่มีสมบัติเป็นไปตามทฤษฎีจลน์ของแก๊สทุกประการเรียกว่า แก๊สอุดมคติ (Ideal gas) โดยปกติแก๊สทั่วไปจะมีสมบัติเคียงกับแก๊สอุดมคติเท่านั้น สำหรับแก๊สที่มีอนุภาคขนาดเล็ก เมื่อควบคุมให้อยู่ในภาวะที่มีปริมาตรมาก ความดันต่ำ และอุณหภูมิสูง จะมีสมบัติใกล้เคียงกับแก๊สอุดมคติมากขึ้น โดยเฉพาะแก๊สเฉื่อยจะมีสมบัติใกล้เคียงกับแก๊สอุดมคติมากจนอาจจัดเป็นแก๊สอุดมคติได้
พลังงานภายในของระบบ (ใช้สัญลักษณ์เป็น E หรือ U) คือ ผลรวมของพลังงานอันเนื่องมาจาก
การเปลี่ยนแปลงพลังงานภายใน มีค่าเท่ากับ งานรวมกับความร้อน
DE = w + q
 | จากที่เราทราบกันว่า ทั้งงานและความร้อนไม่ใช่ฟังก์ชันสภาวะ แล้วนักเรียนคิดว่า การเปลี่ยนแปลงพลังงานภายใน (DE) จะเป็นฟังก์ชันสภาวะหรือไม่ ? |







ไม่มีความคิดเห็น:
แสดงความคิดเห็น